Как вы рассчитываете кДж?
кДж (метрическая система), энергия
в равной степени, что означает кДж / моль?
Тогда сколько килоджоулей в грамме?
Сколько граммов калорий в 1 килоджоуле?
Перевести граммы калорий в килоджоули.
| Грамм калорий | килоджоулей |
|---|---|
| 1 грамм калорий | 4,186.8 килоджоулей |
| 2 грамма калорий | 8,373.6 килоджоулей |
| 5 грамма калорий | 20,934 килоджоулей |
| 10 грамма калорий | 41,868 килоджоулей |
Как перевести кДж в кВт?
Укажите значения ниже, чтобы преобразовать килоджоуль / час [кДж / ч] в киловатт или наоборот.
Килоджоуль / час в Киловатт Таблица преобразования.
| Килоджоуль в час [кДж / ч] | Киловатт |
|---|---|
| 0.1 кДж / ч | 2.77778E-5 кВт |
| 1 кДж / ч | 0.0002777778 кВт |
| 2 кДж / ч | 0.0005555556 кВт |
| 3 кДж / ч | 0.0008333333 кВт |
Опасна ли пищевая добавка
Карбоксиметилцеллюлоза, попадая в организм, не оказывает негативных последствий для здоровья. Ее рассматривают как источник пищевых волокон. Вещество относится к умеренно опасным. Влияние на организм и, в частности, на пищеварительный тракт, мало изучено. Доказано, что употребление более 5 г Е-466 опасно для пищеварения, потому что может вызывать усиление перистальтики. Это провоцирует развитие хронических поносов. Они опасны развитием сильного обезвоживания.
Некоторые российские исследователи утверждают, что это
вещество может обладать канцерогенными свойствами. Впрочем, научные материалы
на эту тему не опубликованы. Неясно, может ли модифицированная целлюлоза
провоцировать аллергические реакции в организме, отравление.
Некоторые специалисты утверждают, что карбоксиметилцеллюлоза, поступающая на отечественные предприятия пищевой промышленности, является генно-модифицированной, а поэтому вредной для здоровья. При этом они путают ГМО (которые действительно вредны) и модифицированное вещество.
Применяемая добавка имеет измененную молекулу целлюлозы. Ее вредность преувеличена. Е-466 не имеет никакого отношения к генной инженерии. Поэтому она и не влияет на геном человека и не провоцирует развитие тяжелых патологий.

Карбоксиметилцеллюлоза – это загуститель, который относится к условно безопасным для здоровья человека. Она разрешена во всех странах. На сегодня нет информации о том, что в каком-либо государстве ее нельзя использовать. Если же у потребителя имеются сомнения относительно безопасности этого химического вещества, он может выбрать альтернативный продукт питания, в котором нет E-466.
Посмотрите видео про Е-добавки:
Тепловой эффект химической реакции
Тепловой эффект – это количества тепла или энергии, которое выделилось или поглотилось во время химической реакции, относительно 1 моль вещества. В химии тепловой эффект обозначают символом Q, измеряют в ккал/моль или кДж/моль. Согласно определению выделяют два типа процессов:
- Экзотермические реакции – протекают с выделением тепла, процесс происходит быстро, в конце реакции записывается, как +Q.
- Эндотермические реакции – протекают с поглощением тепла. Чтобы получить конечный продукт, реагенты нагревают. Процессы занимают много времени. В конце реакции обозначаются, как –Q.
Чем больше прореагирует химического вещества, тем больше выделиться энергии. Следовательно, тепловой эффект зависит от химического вещества в моль вступившего в реакцию.
|
Экзотермическая реакция |
|
| Эндотермическая реакция |
|
По энергии ионизации реагенты в эндотермической реакции находятся выше оси нулевой энергии, т.е. скорость прямой реакции выше, чем обратной и наоборот, в эндотермических реакциях – скорость обратной реакции выше, чем прямой.
Определение теплового эффекта химической реакции
В процессе химической реакции связи в исходных веществах разрываются и образуются новые связи, благодаря чему образуются новые вещества — продукты реакции. Разрыв связи протекает с поглощением энергии, а образование — с выделением, то есть химические реакции сопровождаются энергетическими эффектами.
Как правило, энергия выделяется или поглощается в виде теплоты, поэтому мы говорим, что протекание химической реакции сопровождается тепловым эффектом.
Тепловой эффект химической реакции — это количество теплоты, которое поглощается или выделяется в результате протекания химической реакции.
Если исходные вещества были менее устойчивыми (поглощается небольшое количество энергии), а образуются устойчивые (выделяется большое количество энергии), то в результате химической реакции выделяется тепловой эффект.
И наоборот, образование более устойчивых веществ из менее устойчивых сопровождается поглощением теплоты.
Рассмотрим эти процессы на рисунке:
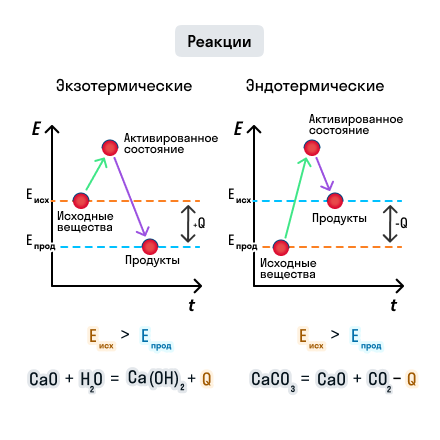
В зависимости от того, выделяется или поглощается теплота, различают два типа химических реакций: экзотермические и эндотермические.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Получить

Характеристики R22 на линии насыщения
| Темпе-ратура, C | Давление, 105Па | Удельный объем | Плотность | Удельная энтальпия, кДж/кг |
Удельная теплота парообра-зования, кДж/кг |
Удельная энтропия, кДж/(кг*К) | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| абсолют-ное | манометри-ческое | жидкости, дм3/кг | пара, дм3/кг | жидкости, кг/дм3 | пара, кг/м3 | жидкости | пара | жидкости | пара | ||
| -100 | 0,020 | -0,993 | 0,636 | 8,008 | 1,570 | 0,124 | 95,87 | 359,35 | 263,48 | 0,5310 | 2,0526 |
| -90 | 0,048 | -0,965 | 0,647 | 3,581 | 1,545 | 0,279 | 105,32 | 364,23 | 258,91 | 0,5840 | 1,9976 |
| -80 | 0,104 | -0,909 | 0,658 | 1,763 | 1,519 | 0,567 | 114,90 | 369,15 | 254,25 | 0,6349 | 1,9512 |
| -70 | 0,205 | -0,808 | 0,669 | 0,9409 | 1,493 | 1,062 | 124,66 | 374,08 | 249,42 | 0,6841 | 1,9118 |
| -60 | 0,374 | -0,639 | 0,682 | 0,5372 | 1,466 | 1,861 | 134,63 | 378,98 | 244,35 | 0,7320 | 1,8783 |
| -50 | 0,643 | -0,370 | 0,695 | 0,3246 | 1,438 | 3,080 | 144,85 | 383,81 | 238,96 | 0,7788 | 1,8496 |
| -41 | 1,002 | -0,011 | 0,707 | 0,2149 | 1,412 | 4,653 | 154,27 | 388,05 | 233,78 | 0,8200 | 1,8270 |
| -40 | 1,049 | +0,036 | 0,709 | 0,2057 | 1,409 | 4,861 | 155,32 | 388,52 | 233,20 | 0,8245 | 1,8247 |
| -30 | 1,635 | +0,622 | 0,724 | 0,1358 | 1,380 | 7,363 | 166,07 | 393,07 | 227,00 | 0,8695 | 1,8030 |
| -20 | 2,448 | +1,435 | 0,740 | 0,09284 | 0,349 | 10,771 | 177,10 | 397,42 | 220,32 | 0,9137 | 1,7840 |
| -10 | 3,543 | +2,530 | 0,758 | 0,06534 | 0,317 | 15,304 | 188,40 | 401,53 | 213,13 | 0,9572 | 1,7670 |
| 4,976 | +3,963 | 0,778 | 0,04714 | 0,284 | 21,213 | 200,00 | 405,36 | 205,36 | 1,0000 | 1,7518 | |
| 10 | 6,807 | +5,794 | 0,800 | 0,03471 | 0,250 | 28,810 | 211,90 | 408,86 | 196,96 | 1,0423 | 1,7378 |
| 20 | 9,099 | +8,086 | 0,824 | 0,02600 | 0,213 | 38,461 | 224,14 | 411,97 | 187,83 | 1,0841 | 1,7248 |
| 30 | 11,92 | +10,90 | 0,851 | 0,01974 | 0,173 | 50,658 | 236,75 | 414,62 | 177,87 | 1,1256 | 1,7123 |
| 40 | 15,34 | +14,32 | 0,883 | 0,01514 | 0,131 | 66,050 | 249,81 | 416,69 | 166,88 | 1,1670 | 1,6999 |
| 50 | 19,42 | +18,40 | 0,921 | 0,01167 | 0,084 | 85,689 | 263,43 | 418,01 | 154,58 | 1,2087 | 1,6870 |
| 60 | 24,27 | +23,25 | 0,968 | 0,009001 | 0,032 | 111,098 | 277,81 | 418,30 | 140,49 | 1,2511 | 1,6728 |
| 70 | 29,96 | +28,94 | 1,030 | 0,006889 | 0,970 | 145,158 | 293,30 | 417,07 | 123,77 | 1,2952 | 1,6559 |
| 80 | 36,62 | +35,60 | 1,118 | 0,005149 | 0,894 | 194,212 | 310,74 | 413,22 | 102,48 | 1,3432 | 1,6334 |
| 90 | 44,43 | +43,41 | 1,282 | 0,003564 | 0,780 | 280,583 | 332,99 | 403,03 | 70,04 | 1,4027 | 1,5956 |
Общее описание R22
R22 это хладагент среднего давления, такой как аммиак, но его преимущество заключается в меньшем соотношении давлений. Так могут достигаться двухступенчатого температуры от –60°C до –75°C. Поршневой компрессор (также ротационный и особенно винтовой компрессор) используются обычно для R22, причем значительный процент составляют герметики. При низких температурах, т.е. больших рабочих объемах, используются также турбокомпрессоры. R22 это возможный переходный хладагент в качестве заменяемого хладагента для фреонов R12 и R502 при применении при низких температурах и в смесях для всего диапазона применения R12. При этом следует учесть, что объемная холодопроизводительность по сравнению с R12 больше примерно на 60%.
R22 является известным и широко исследованным хладагентов. В настоящее время он является наиболее часто используемым хладагентом, спектр его применения очень широкий: обычный диапазон температуры испарения –40°C до – 5°C для применения в буфетах и шкафах-морозилках, морозильных ларях, кондиционерах, холодильных камерах, камерах холода в научных целях, как транспортировочного холода, торгового холода (особенно в супермаркетах), промышленного холода, а также и в тепловых насосах.
R22 не горючий и в токсикологическом отношении безопасен (ПДК 500 объемн. ppm, ориентировочное предельное значение для ЕС 1000 объемн. ppm). Показатель ODP (распределенная обработка в открытой системе) по сравнению с R12 сокращен на 94.5%. Из-за остаточного показателя ODP в 5.5% R22 можно характеризовать как “опасный для окружающей среды ”.
В условиях холодильных машин R22 термически и химически устойчив. Совместимость с металлами сравнима с R12. Обычными конструкционными материалами являются: медь, латунь, монель-металл, никель, чугун, сталь и алюминий. От магния, свинца, цинка и сплавов алюминия с содержанием магния более 2 % массы следует отказаться.
По сравнению с пластмассами и эластомерами R22 более агрессивен, чем R12 и ведет нередко к усиленному разбуханию. Хлорпренкаучук (CR), хлорсульфонированный полиэтилен (CSM) и политетрафторэтилен (PTFE) могут использоваться, а акрилнитрил-бутадиенкаучук (NBR) и фторосодержащие каучуки (FKM-типы) использовать нельзя.
R22 и минеральные масла при более высоких температурах полностью смешиваются, но при более низких лишь ограниченно. Широкий концентрационный предел совместимости при установках с низкими температурами р может привести к трудностям при возврате масла из испарителя. Поэтому для таких случаев рекомендуется эффективный маслоотделитель или использование полусинтетических масел.
Гигакалории или киловатты
Разберемся окончательно, в чем отличие этих единиц измерения. Пусть у нас имеется нагревательный прибор, например, чайник. Возьмем 1 литр холодной воды из-под крана (температура t1=15°C) и вскипятим ее (нагреем до температуры t2=100°C). Электрическая мощность чайника — P=1,5 кВт. Сколько тепла поглотит вода? Чтобы это узнать, применим знакомую нам формулу, при этом учтя, что масса 1 литра воды m=1 кг: Q=4183 [Дж/(кг*°C)]*1 кг*(100°С-15°С)=355555 Дж=84922,8528 кал≈85 ккал.
За какое время вскипит чайник? Пусть вся энергия электрического тока уйдет на нагрев воды. Тогда неизвестное время мы найдем, используя энергетический баланс: «Энергия, расходуемая чайником, равна энергии, поглощаемой водой (без учета потерь)». Энергия, расходуемая чайником за время τ, равна P*τ. Энергия, поглощаемая водой, равна Q. Тогда на основе баланса получим P*τ=Q. Отсюда время нагрева чайника составит: τ=Q/P=355555 Дж/1500 Вт≈237 с≈4 мин. Количество теплоты, переданное чайником воде за единицу времени — это и есть его тепловая мощность. Она составит в нашем случае величину Q/τ=84922,8528 кал/237 с≈358 кал/с=0,0012888 Гкал/ч.
Таким образом, кВт и Гкал/ч — это единицы мощности, а Гкал и МДж — единицы теплоты и энергии. Как подобные расчеты можно применить на практике? Если нам приходит квитанция об оплате отопления, то мы платим за тепло, которое снабжающая организация поставляет нам по трубам. Это тепло учитывается в гигакалориях, т. е. в количестве теплоты, потребленном нами за расчетный период. Нужно ли переводить эту единицу в джоули? Конечно, нет, потому что мы просто платим за конкретное число гигакалорий.
Однако часто бывает необходимо выбрать для дома или квартиры те или иные отопительные приборы, например, кондиционер, радиатор, бойлер или газовый котел. В связи с чем требуется заранее знать тепловую мощность, требуемую для обогрева помещения. Зная эту мощность, можно подобрать соответствующий прибор. Она может быть указана как в кВт, так и в Гкал/ч, а также в единицах BTU/h (British Thermal Unit — Британская Термическая Единица, h — час). Следующая памятка поможет вам перевести кВт в Гкал/ч, кВт в BTU/h, Гкал в кВт*ч и BTU в кВт*ч.
Памятка 2
- один Вт=одному Дж/с=0,2388459 кал/с=859,8452 кал/ч=0,8598 ккал/ч;
- один кВт=одному кДж/с=1000 Дж/с=238,8459 кал/с=859845,2279 кал/ч=0,00085984523 Гкал/ч;
- один МВт=один МДж/с=один млн Дж/с=1000 кВт=238845,8966 кал/с=0,85984523 Гкал/ч;
- одна Гкал/ч=один млрд кал/ч=1163000 Вт=1163 кВт=1,163 МВт=3968156 BTU/h;
- одна BTU/h=0,2931 Вт=0,0700017 кал/с=252,0062 кал/ч=0,2520062 ккал/ч;
- один Вт=3,412 BTU/h, один кВт=3412 BTU/h, один МВт=3412000 BTU/h.
Как определяется единица BTU/h и для чего она используется? 1 BTU — это количество теплоты, необходимое для нагревания 1 фунта воды на 1° по Фаренгейту (°F). Эта единица измерения используется в основном для обозначения тепловой мощности установок, таких, например, как кондиционеры.
Практика
Рассмотрим несколько термохимических расчетов для типовых заданий.
Задача 1
Рассчитайте количество теплоты, выделившейся в результате реакции образования метана, термохимическое уравнение которой —
C(тв) + 2H2 (г) = CH4 (г) + 76 кДж,
из: а) 0,3 моля углерода; б) 2,4 г углерода; в) 2,24 л водорода.
Решение.
Важно помнить, что количество теплоты, которая выделяется в результате реакции, пропорционально количеству вещества, вступившего в реакцию. а) Из термохимического уравнения видно, что при взаимодействии 1 моля С выделяется 76 кДж, тогда при взаимодействии 0,3 моля С выделяется x кДж
а) Из термохимического уравнения видно, что при взаимодействии 1 моля С выделяется 76 кДж, тогда при взаимодействии 0,3 моля С выделяется x кДж.
Составим уравнение и решим его:
1 моль × х = 76 кДж × 0,3 моля;
.
б) Для начала найдем количество вещества прореагировавшего углерода. Для этого разделим его массу m на молярную массу M:
.
Молярная масса углерода равна 12 г/моль (значение из таблицы Менделеева).
Тогда .
В соответствии с термохимическим уравнением при взаимодействии 1 моля С выделяется 76 кДж, тогда при взаимодействии 0,2 моля выделяется х кДж.
Данной пропорции соответствует уравнение:
1 моль × х = 76 кДж × 0,2 моля;
.
в) Для начала найдем количество вещества вступившего в реакцию водорода. Для этого разделим его объем V на молярный объем Vm:
.
Молярный объем любого вещества равен 22,4 л/моль.
Тогда .
В соответствии с термохимическим уравнением при взаимодействии 2 молей H выделяется 76 кДж, тогда при взаимодействии 0,1 моля выделяется х кДж.
Данной пропорции соответствует уравнение:
1 моль × х = 76 кДж × 0,1 моля;
.
Задача 2
В результате реакции, термохимическое уравнение которой —
2H2 (г) + O2 (г) = 2H2O (г) + 484 кДж,
выделилось 1 360 кДж. Вычислите: а) объем (н. у.) вступившего в реакцию кислорода; б) массу образовавшейся воды.
Решение.
а) В соответствии с термохимическим уравнением при взаимодействии
1 моля кислорода выделяется 484 кДж, тогда при взаимодействии
х молей кислорода выделяется 1 360 кДж.
Этой пропорции соответствует уравнение:
1 моль × 1 360 кДж = 484 кДж × х молей;
.
Найдем объем вступившего в реакцию кислорода, воспользовавшись формулой:
V = n(H) × Vm, где Vm — молярный объем;
V(H) = 2,81 моля × 22,4 л/моль = 62,95 л.
б) В соответствии с термохимическим уравнением при взаимодействии
2 молей воды выделяется 484 кДж, тогда при взаимодействии
х молей кислорода выделяется 1 360 кДж.
Этой пропорции соответствует уравнение:
2 моля × 1 360 кДж = 484 кДж × х молей;
.
Найдем объем вступившего в реакцию кислорода, воспользовавшись формулой:
m(H2O) = n(H2O) × M(H2O), где M — молярная масса;
M(H2O) = 1 × 2 + 16 × 1 = 18 г/моль;
m(H2O) = 5,62 моля × 18 г/моль = 101,16 г.
Еще больше задач, да еще и в интерактивном формате — на онлайн-курсах по химии в школе Skysmart.
Что такое тепловой эффект химической реакции
Химические реакции практически всегда сопровождаются какими-либо тепловыми явлениями.
Так, горение, нейтрализация кислоты щелочью, реакция металла (например, магния) с хлором и т.д. происходят с выделением достаточного количества тепла. А вот, чтобы разложить мел (карбонат кальция), необходимо все время его нагревать. Если нагревание (то есть подвод тепла) прекратить, то и реакция тоже прекратится. Это говорит о том, что разложение карбоната кальция идет с поглощением тепла.
В чем же дело? Любое вещество является продуктом взаимодействия частиц (атомов или ионов). В ходе образования вещества энергия взаимодействия как бы прячется в химических связях (ковалентных, ионных). Это так называемая , которая частично высвобождается в ходе химического взаимодействия. Она же – тепловой эффект реакции. Измеряя его, можно судить о том, как изменилась внутренняя энергия вещества.
Тепловой эффект химической реакции обозначают буквой Q и измеряют в кДж (или в ккал в случае, когда речь идет об обеспечении энергией живых организмов).
Если в результате химического взаимодействия теплота выделяется, то это ; если теплота поглощается – .
Расчеты по термохимическим уравнениям
В термохимических расчетах чаще используются уже готовые термохимические уравнения. Требуется найти массы/объемы образующихся/исходных веществ, количество выделившейся/поглощенной теплоты.
Рассмотрим несколько примеров.
Пример 4. По термохимическому уравнению: N2(г.) + O2(г.) = 2NO(г.) – 180,7 кДж вычислите тепловой эффект реакции, в которой участвует азот объемом 5,6 л (при н.у.).
Поскольку реакция эндотермическая, то поглотится 45,2 кДж энергии.
Пример 5. Тепловой эффект реакции горения этилена составляет 1400 кДж (в расчете на 1 моль этилена). Сколько этилена (при н.у.) необходимо сжечь, чтобы получить 560 кДж теплоты?
Пример 6. Пользуясь термохимическим уравнением сгорания пропана
C3H8 + 5O2 = 3CO2 + 4H2O + 2220,03 кДж,
определите количество выделившейся теплоты, если в реакцию вступит кислород: а) массой 16 г; б) объемом 67,2 л; в) количеством вещества 2,5 моль. Сколько оксида углерода (IV) по объему и по массе получится, если при горении пропана выделится 277,5 кДж теплоты?
Если вы готовитесь к выпускному экзамену (ЕГЭ по химии), то имейте ввиду, что вычислить тепловой эффект реакции требует задание № 27 (версия 2022 года).
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
или на Одноклассниках
Пожалуйста, оцените публикацию. Большая просьба, если вы оцениваете публикацию от 1 до 3 звезд, обязательно оставьте свой комментарий с указанием того, что не так с этой публикацией. Мы постараемся устранить недостатки.
Ваше мнение для нас важно!
Где применяется пищевая добавка Е 466
Это вещество применяется в широких сферах деятельности человека. Оно позволяет решать многие технологические задачи в производстве продуктов:
- создание различных растворов с определенной
степенью густоты; - создание псевдопластических растворов;
- образование гелей.
Вот в каких продуктах содержится этот загуститель:
- продукты быстрого приготовления;
- соусы;
- мороженое;
- начинки для кондитерских изделий;
- желе;
- мармелады;
- плавленые сырки;
- молочные десерты;
- сливки и сметана;
- ароматизированные йогурты;
- рыбные консервы.
Кроме того, карбоксиметилцеллюлоза входит в состав оболочек
для разнообразных изделий из мяса и рыбы. Добавка имеет полезное свойство: она
удерживает влагу, защищает от высыхания пищевого продукта. При размораживании
пищевые волокна не поражаются.
Потребителям необходимо знать, сколько карбоксиметилцеллюлозы может безопасно находиться в продукте. Нормальное количество – 8 г на килограмм. В составе оболочки для пищевого продукта его может быть несколько больше.
Такое вещество может быть и в составе некоторых косметических продуктов и средств бытовой химии:
- зубных пастах;
- кремах для бритья;
- гелей для душа;
- шампунях.
В фармацевтической промышленности добавка применяется для создания защитной оболочки для таблеток. Карбоксиметилцеллюлоза обнаруживается и в глазных каплях.

История
«Такую тепловую единицу, если она будет сочтена приемлемой, я думаю, с большим уместностью можно было бы назвать джоуль, в честь человека, который так много сделал для разработки динамической теории тепла».
На втором Международном электрическом конгрессе 31 августа 1889 года джоуль был официально принят наряду с ваттом и квадрантом (позже переименованным в генри ). Джоуль умер в том же году, 11 октября 1889 г. На четвертом конгрессе (1893 г.) были определены «международный ампер» и «международный ом» с небольшими изменениями в спецификациях для их измерения, при этом «международный джоуль» был единица, производная от них.
Определение джоуля как J = кг⋅м 2 ⋅с −2 оставалось неизменным с 1946 года, но джоуль как производная единица унаследовал изменения в определениях второго (в 1960 и 1967) метра (в 1983 году). ) и килограмм ( в 2019 году ).
Закон Гесса
В 1840 году русский ученый описал закон термохимии, который до сих пор используется. Его называют законом Гесса:
Тепловой эффект зависит от агрегатного состояния начальных и конечных продуктов, промежуточные стадии, не влияют.
Это правило помогает узнать тепловой эффект промежуточных стадий. Он будет равен разнице между начальным и конечным значением. По сумме переходных реакций выясняют общий тепловой эффект.
Тепловой эффект химических реакций
Количество теплоты, которые выделяется или поглощается в результате реакции, называют тепловым эффектом данной реакции.
- обычно обозначают Q
Qp = Qкон. — Qисх.
- выражают в Дж или кДж
2H2(г) + O2(г) = 2H2O(ж) + 484 кДж
Смотри также:
- Классификация химических реакций в неорганической и органической химии
- Скорость химической реакции, ее зависимость от различных факторов
- Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
- Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты
- Реакции ионного обмена
- Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
- Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее
- Электролиз расплавов и растворов (солей, щелочей, кислот)
- Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии
Значение слова «килоджоуль»

Делаем Карту слов лучше вместе
Я стал чуточку лучше понимать мир эмоций.
Вопрос: вытерпеть — это что-то нейтральное, положительное или отрицательное?
Предложения со словом «килоджоуль»
Дополнительно
Предложения со словом «килоджоуль»
Максимально за час может выделиться от 1 до 3,5 литра пота, что эквивалентно отдаче 2500–8700 килоджоулей тепла.
– Может, миллиард килоджоулей энергии скопились в одном месте и решили, что они сами по себе, а всё остальное само по себе?
В конце концов, я сам пострадал – когда на расстоянии вытянутой руки разряд в три килоджоуля разносит чей-то череп, это, мягко говоря, неприятно.
Правописание
Карта слов и выражений русского языка
Онлайн-тезаурус с возможностью поиска ассоциаций, синонимов, контекстных связей и примеров предложений к словам и выражениям русского языка.
Справочная информация по склонению имён существительных и прилагательных, спряжению глаголов, а также морфемному строению слов.
Сайт оснащён мощной системой поиска с поддержкой русской морфологии.
Что такое Е466
Так называется карбоксиметилцеллюлоза (или Carboxymethyl cellulose). Относится к загустителям продуктов. Раствор этого вещества – клейкая и вязкая жидкость. Степень вязкости жидкости полностью зависит от количества гидроксильных групп. Нормальны показатель замещения – это от 0,65 до 0,95.
Добавление карбокисметилцеллюлозы в воду позволяет получать растворы разной степени вязкости. Польза этого свойства в том, что производитель может значительно улучшить органолептические и вкусовые качества продукта питания. С химической точки зрения Е 466 – это полиэлектролит.
В лаборатории добавка E 466 получается путем реакции монохлоруксусной кислоты и
алкилцеллюлозы.
Главные свойства добавки:
- цвет – белый, иногда светло-бежевый;
- по внешнему виду это волокнообразный порошок (иногда гранулы);
- запаха у этого вещества нет;
- хорошо растворяет в холодной, горячей воде и щелочах;
- вкус – отсутствует;
- хорошо устойчиво к свету.
На предприятия пищевой промышленности это вещество поступает в бумажных многослойных мешках, барабанах. В них обязательно находится полиэтиленовый вкладыш для защиты от поступления влаги.

составить термохимическое уравнение
Взаимодействие веществ принято отражать (записывать) с помощью химического уравнения. Если в таком уравнении указан тепловой эффект, то тогда уравнение будет называться .
Например, обычное уравнение реакции:
А это уже термохимическое уравнение данной реакции:
Уравнение говорит о том, что при взаимодействии 1 моля PbO с 1 молем СО, идущем с образованием 1 моля Pb и 1 моля CO2, выделяется 64 кДж теплоты.
Особенности термохимических уравнений:
1) указывается агрегатное состояние веществ (однако, если все вещества находятся в одном агрегатном состоянии, то его могут не указывать);
2) указывается тепловой эффект реакции в соответствии с ее стехиометрией (то есть, в соответствии с правильно расставленными коэффициентами);
3) тепловой эффект записывается в левой части уравнения;
4) если речь идет о горении вещества, то уравнение составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции называется
5) если речь идет об образовании вещества, то уравнение также составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции будет называться
А теперь разберем несколько задач, требованием которых является составление термохимического уравнения.
Что нужно сделать для решения таких задач?
1) записать условие задачи;
2) составить уравнение реакции;
3) вычислить ее тепловой эффект;
4) записать полученное значение теплового эффекта в уравнение реакции.
Пример 1. Кальций массой 8 г сгорает с выделением 127 кДж теплоты. Напишите термохимическое уравнение (тху) реакции.
Пример 2. При разложении 6,86 г оксида ртути (II) тратится 3,64 кДж тепловой энергии. Напишите термохимическое уравнение (тху) реакции.
Пример 3. Реакция 6 г углерода с водородом приводит к выделению 37,42 кДж теплоты. Напишите термохимическое уравнение (тху) реакции образования метана.
Примеры задач
Задача 1
45 г глюкозы (С6Н12О6) подвергли обработке избытком кислорода, в результате чего выделилось 700 кДж энергии. Выясните значение теплового эффекта? Реакция протекала по следующей формуле:
С6Н12О6 (тв) + 6О2(газ) = 6СО2(газ) + 6Н2О(газ) + 700 кДж
Решение:
Найдем химическое количество глюкозы:
n(C6H12O6) = m(C6H12O6) :M(C6H12O6) = 45 г : 180 г/моль = 0,25 моль;
Получается, что при взаимодействии 0,25 моль вещества образуется 700 кДж энергии. Тепловой эффект приравнивают к значению 1 моль. Следовательно, составим пропорцию:
0,25 моль – 700 кДж
1 моль – Q кДж
Q = (1* 700) : 0,25 = 700 : 0,25 = 2800 кДж
Задача 2
Представлено термохимическое уравнение, в процессе которого выделилось 3330 кДж энергии, образовалось 68 г Al2O3.Рассчитайте какое количества тепла выделилось, уравнение имеет следующий вид:
3Fe3O4 (тв) + 8A(тв)l = 9 Fe(тв) + 4Al2O3(тв) + 3300Дж
Решение:
Найдем химическое количество оксида алюминия(III):
n(Al2O3)= m(Al2O3 : M(Al2O3) = 68 г : 102 г/моль = 0,677 моль;
Исходя из исходного уравнения, для получения 4 моль оксида алюминия(III) расходуется 3330 кДж энергии, для того, чтобы выяснить, сколько выделяется тепла для 68 г, нужно составить пропорцию:
4 моль – 3330 кДж
0,667 моль – Q кДж
Q = (0,667 * 3330) : 4 = 2,221 : 4 = 555 кДж;
Какое упражнение сжигает больше всего калорий за 30 минут?
Бег даже в медленном темпе сжигает много калорий за 30 минут. В среднем бег сжигает от 10.8 до 16 калорий в минуту и ставит его на первое место в списке тренировок, которые сжигают больше всего калорий. Чтобы увеличить сжигание калорий, увеличьте интенсивность или увеличьте интервалы спринта.
Как я могу сжигать 1500 калорий в день? Какие упражнения помогут сжечь 1500 калорий в день?
- Бег. Бег — одно из самых эффективных упражнений для сжигания калорий.
- Езда на велосипеде. Езда на велосипеде — еще один зверь, сжигающий калории.
- Плавание. …
- Скалолазание.
Является ли калория единицей энергии?
Калория единица измерения энергии. … Калория (ккал) – это количество энергии, необходимое для повышения температуры 1 килограмма воды на 1 градус Цельсия. Иногда содержание энергии в пище выражается в килоджоулях (кДж), метрической единице. Одна ккал равна 4.184 кДж.
Джоуль — это моль? Джоуль на моль (обозначение: Дж моль-1 или Дж / моль) составляет производная единица измерения энергии в системе СИ на количество материала. … Так как 1 моль = 6.02214076 × 1023 частиц (атомы, молекулы, ионы и т. д.), 1 джоуль на моль равен 1 джоуля, деленному на 6.02214076 × 1023 частицы, 1.66054×10-24 джоуль на частицу.
Почему родинка 6.022х10 23?
Один моль равен 6.022 × 1023 единицы. Моль — важная единица измерения, потому что в периодической таблице один моль вещества равен его атомная масса в граммах. … Это означает, что 6.022 × 1023 атомы углерода (или молекулы) весят 12.01 грамма.
Как называется 6.022х10 23? Авогадро число, количество единиц в одном моле какого-либо вещества (определяется как его молекулярная масса в граммах), равное 6.02214076 × 1023. Единицами могут быть электроны, атомы, ионы или молекулы, в зависимости от природы вещества и характера реакции (если таковая имеется). См. Также закон Авогадро.
Физические свойства R22
| Параметр |
Единица измерения |
Значение | ||
|---|---|---|---|---|
|
При -15°С (насыщ.жидк.) |
При 25°С (насыщ.жидк.) |
При 25°С (насыщ.пар) |
||
| Химическая формула | — | CHClF2 | ||
| Молярная масса | кг/кмоль | 86.468 | ||
| Температура плавления | °С | -157.4 | ||
| Температура кипения при атм. давлении (101кПа) | °С | -40.85 | ||
| Критическая температура | °С | 96.13 | ||
| Критическое давление | МПа | 4.986 | ||
| Критическая плотность | кг/м3 | 512.8 | ||
| Вязкость | мПа·с | 0.247 | 0.160 | 0.013 |
| Теплопроводность | Вт/(м·К) | 0.103 | 0.086 | 0.011 |
| Средняя уд.теплоемкость | кДж/(кг·К) | — | 1.260 | 0.864 |
| Отношение cp/cv | — | — | — | 1.38 |
| Плотность | кг/м3 | — | 1191 | 44.23 |
| Энтальпия испарения | кДж/кг | — | 182.5 | — |
Границы взравоопасности в воздухе при 25°С и атмосферном давлении (101кПа): отсутствуют.
1 кДж равен 1 калории?
Преобразовать килоджоули в калории
Этот калькулятор работает в диапазоне от калорий до килоджоулей, где 1 калория равна 4.184 килоджоуля, округленное до ближайшего целого числа.
Как перевести кДж в кВт?
Чтобы преобразовать килоджоули в киловатт-час, разделите энергию на коэффициент преобразования. Энергия в киловатт-часах равна равно килоджоулей, разделенных на 3,600.
Сколько кДж я должен есть в день? Сколько килоджоулей я должен съедать в день? В среднем взрослому человеку требуется около 8,700 килоджоулей (кДж) в день для поддержания здорового веса. Это среднее число, которое варьируется в зависимости от многих факторов, в том числе от того, насколько мы активны, нашего возраста, пола, роста и веса. Затем наше тело использует эту энергию для поддержания функционирования нашего тела.
Полезно ли сжигать 4000 калорий в неделю? Сжигание 4,000 калорий с помощью целенаправленных упражнений, по-видимому, является точкой отсечки (да, вы можете немного меньше или больше, но суть в том, что нам нужно где-то провести черту), после которой здоровье, включая иммунную функцию и нагрузку окислительного стресса, и качество жизни, включая свободное время, уровень энергии и…
Термохимическое уравнение
Химические уравнения, в которых отображается тепловой эффект называются термохимическими. При записи в скобках обязательно указывают агрегатное состояние вещества: твердое, жидкое, газообразное и другое. Коэффициенты прописываются в условии: дробные или цельные числа.
При расчете учитывают температуру и давление, при которых протекает процесс. Если в условиях задачи не прописаны значения, то их принимают как стандартные: температура 278К, а давление 110,3 кПа.
В конце записи химического уравнения записывают значение Q, которое берут в справочнике, отдельно для каждого вещества. Энергия представлена в кДж в стандартных условиях. Применяется для расчета по формулам.
Сколько кДж в моль?
Приставка «кило» означает 1,000, поэтому один кДж = 1,000 Дж. Поскольку энергии, связанные с одной молекулой или атомом, довольно малы, нам часто легче обсуждать энергию, содержащуюся в одном моле вещества, следовательно, «на моль». Чтобы получить энергию одной молекулы, разделите кДж/моль на число Авогадро, 6.022 х 1023.
Также является ккал единицей энергии? Одна килокалория (1 ккал или 1000 калорий) — это количество тепла (энергии), необходимое для повышения температуры одного кг воды на один градус Цельсия (°C). Стандартная единица СИ для энергия Джоуль (Дж). Одна ккал составляет примерно 4.18 кДж (это немного зависит от температуры).
Ккал такой же, как кал?
«Калория», которую мы называем в еде, на самом деле является килокалорией. Одна (1) килокалория равна одной (1) калории. (верхний регистр С). Килокалория – это количество тепла, необходимое для повышения температуры одного килограмма воды на один градус Цельсия.
Как перевести ккал в калории? Чтобы преобразовать измерение килокалорий в измерение калорий, умножьте энергию на коэффициент преобразования. Энергия в калориях равно килокалориям, умноженным на 1,000.


































