Тепловой эффект химической реакции
Тепловой эффект – это количества тепла или энергии, которое выделилось или поглотилось во время химической реакции, относительно 1 моль вещества. В химии тепловой эффект обозначают символом Q, измеряют в ккал/моль или кДж/моль. Согласно определению выделяют два типа процессов:
- Экзотермические реакции – протекают с выделением тепла, процесс происходит быстро, в конце реакции записывается, как +Q.
- Эндотермические реакции – протекают с поглощением тепла. Чтобы получить конечный продукт, реагенты нагревают. Процессы занимают много времени. В конце реакции обозначаются, как –Q.
Чем больше прореагирует химического вещества, тем больше выделиться энергии. Следовательно, тепловой эффект зависит от химического вещества в моль вступившего в реакцию.
|
Экзотермическая реакция |
|
| Эндотермическая реакция |
|
По энергии ионизации реагенты в эндотермической реакции находятся выше оси нулевой энергии, т.е. скорость прямой реакции выше, чем обратной и наоборот, в эндотермических реакциях – скорость обратной реакции выше, чем прямой.
Сколько калорий должна есть девочка-подросток?
В раннем подростковом возрасте организму требуется больше калорий, чем в любое другое время жизни. Мальчикам требуется в среднем 2,800 калорий в день. Девочки требуют в среднем 2,200 калорий в день.
тогда что такое формула джоуля? Форма неравенства: работа (джоули) = сила (ньютоны) x расстояние (метры),… Один джоуль определяется как количество работы, выполненной при приложении силы в один ньютон на расстоянии одного метра.
Что такое 1e 12? Научное обозначение и метрические аффиксы
| Чтобы ввести этот номер | Используйте этот метрический аффикс | Используйте это обозначение E |
|---|---|---|
| 0.000000000001 | 1p (пико) | 1e-12 |
| 1,000 | 1k (кило) | 1e3 |
| 1,000,000 | 1 млн (мега) | 1e6 |
| 1,000,000,000 | 1G (гига) | 1e9 |
Как найти другие величины из этого равенства?
Во-первых, количество теплоты. Формула будет выглядеть таким образом: Q = с * m * (t2 – t1). Только в нее необходимо подставлять величины в единицах, входящих в СИ. То есть масса в килограммах, температура — в градусах Цельсия. Это формула № 2.
Во-вторых, массу вещества, которое остывает или нагревается. Формула для нее будет такой: m = Q / (c * (t2 – t1)). Это формула под № 3.
В-третьих, изменение температуры Δt = t2 – t1 = (Q / c * m). Знак «Δ» читается как «дельта» и обозначает изменение величины, в данном случае температуры. Формула № 4.
В-четвертых, начальную и конечную температуры вещества. Формулы, справедливые для нагревания вещества, выглядят таким образом: t1 = t2 — (Q / c * m), t2 = t1 + (Q / c * m). Эти формулы имеют № 5 и 6. Если в задаче идет речь об охлаждении вещества, то формулы такие: t1 = t2 + (Q / c * m), t2 = t1 — (Q / c * m). Эти формулы имеют № 7 и 8.
Задача №3
Какая масса древесного угля при сгорании дает столько же энергии, сколько выделяется при сгорании четырех литров бензина?
Дано:$V_б = 4 \space л$$\rho_б = 710 \frac{кг}{м^3}$$q_б = 4.6 \cdot 10^7 \frac{Дж}{кг}$$q_у = 3.4 \cdot 10^7 \frac{Дж}{кг}$
СИ:$V_б = 4 \cdot 10^{-3} \space м^3$
$m_у — ?$
Показать решение и ответ
Скрыть
Решение:
Некоторая масса древесного угля при сгорании даст столько же энергии, сколько выделяется при сгорании данного объема бензина: $Q_у = Q_б$.
Формула для расчета количества теплоты, выделившегося при сгорании древесного угля:$Q_у = q_у m_у$.
Формула для расчета количества теплоты, выделившегося при сгорании бензина:$Q_б = q_б m_б$.
Масса бензина нам неизвестна, но известна его плотность и объем. Плотность по определению: $\rho_б = \frac{m_б}{V_б}$.Тогда масса бензина будет равна: $m_б = \rho_б V_б$.
Подставим в формулу для расчета количеста теплоты, выделившегося при сгорании бензина:$Q_б = q_б \rho_б V_б$.
Теперь приравняем эти две формулы для нахождения количества теплоты (для бензина и для древесного угля):$q_у m_у = q_б \rho_б V_б$.
Выразим отсюда массу древесного угля:$m_у = \frac{q_б \rho_б V_б}{q_у}$.
Рассчитаем ее:$m_у = \frac{4.6 \cdot 10^7 \frac{Дж}{кг} \cdot 710 \frac{кг}{м^3} \cdot 4 \cdot 10^{-3} \space м^3}{3.4 \cdot 10^7 \frac{Дж}{кг}} = \frac{13 \space 064 \cdot 10^4 \space Дж}{3.4 \cdot 10^7 \frac{Дж}{кг}} \approx 3 \space 842 \cdot 10^{-3} \space кг \approx 3.8 \space кг$.
Ответ: $m_у \approx 3.8 \space кг$.
Задача №9
КПД шахтной печи составляет $60 \%$. Сколько надо древесного угля, чтобы нагреть $10 \space 000 \space кг$ чугуна от $20 \degree C$ до $1100 \degree C$?
Дано:$\eta = 60 \% = 0.6$$m_ч = 10 \space 000 \space кг$$c_ч = 540 \frac{Дж}{кг \cdot \degree C}$$t_1 = 20 \degree C$$t_2 = 1100 \degree C$$q_у = 3.4 \cdot 10^7 \frac{Дж}{кг}$
$m_у — ?$
Показать решение и ответ
Скрыть
Решение:
Формула для КПД шахтной печи:$\eta = \frac{Q _ч}{Q_у}$, где $Q_ч$ — количество теплоты, которое необходимо сообщить чугуну, чтобы нагреть его, $Q_у$ — количество теплоты, которое выделится при сгорании древесного угля неизвестной массы.
Выразим отсюда $Q_у$:$Q_у = \frac{Q_ч}{\eta}$.
Количество тепла, которое выделится при сгорании древесного угля, определяется по формуле:$Q_у = q_у m_у$.
Выразим отсюда массу древесного угля:$m_у = \frac{Q_у}{m_у}$.
Подставим сюда найденное выражение для $Q_у$:$m_у = \frac{\frac{Q_ч}{\eta}}{q_у} = \frac{Q_ч}{\eta \cdot q_у}$.
Рассчитаем отдельно величинe $Q_ч$.Количество теплоты, необходимое для нагревания чугуна:$Q_ч = = c_ч m_ч (t_2 — t_1)$.
Рассчитаем его:$Q_ч = 540 \frac{Дж}{кг \cdot \degree C} \cdot 10 \space 000 \space кг \cdot (1100 \degree C — 20 \degree C) = 0.54 \cdot 10^7 \frac{Дж}{кг} \cdot 1080 \degree C = 583.2 \cdot 10^7 \space Дж$.
Теперь мы можем рассчитать необходимую массу древесного угля:$m_у = \frac{583.2 \cdot 10^7 \space Дж}{0.6 \cdot 3.4 \cdot 10^7 \frac{Дж}{кг}} = \frac{583.2 \space кг}{2.04} \approx 286 \space кг$.
Ответ: $m_у \approx 286 \space кг$.
Задача №8
Найдите КПД примуса, в котором при нагревании $4 \space л$ воды от $20 \degree C$ до $75 \degree C$ сгорело $50 \space г$ керосина.
Дано:$V_в = 4 \space л$$m_к = 50 \space г$ $t_1 = 20 \degree C$$t_2 = 75 \degree C$$c_в = 4200 \frac{Дж}{кг \cdot \degree C}$$\rho_в = 1000 \frac{кг}{м^3}$$q_к = 4.6 \cdot 10^7 \frac{Дж}{кг}$
СИ:$V_в = 4 \cdot 10^{-3} м^3$$m_к = 0.05 \space кг$
$\eta — ?$
Показать решение и ответ
Скрыть
Решение:
КПД определяется по формуле:$\eta = \frac{Q _п}{Q_з} \cdot 100\%$.
В нашем случае полезное количество теплоты — это количество теплоты, которое требуется для нагревании воды, а затраченное количество теплоты — это та энергия, которая выделялась при сгорании керосина.Тогда формула для КПД примет вид:$\eta = \frac{Q _в}{Q_к} \cdot 100\%$.
Рассчитаем отдельно величины $Q_в$ и $Q_к$.Количество теплоты, необходимое для нагревания воды:$Q_в = = c_в m_в (t_2 — t_1)$.
Выразим массу воды через ее плотность и объем: $m_в = \rho_в V_в$.Подставим ее в формулу и рассчитаем количество теплоты:$Q_в = c_в \rho_в V_в (t_2 — t_1)$,$Q_в = 4200 \frac{Дж}{кг \cdot \degree} \cdot 1000 \frac{кг}{м^3} \cdot 4 \cdot 10^{-3} \space м^3 \cdot (75 \degree C — 20 \degree C) = 16 \space 800 \frac{Дж}{\degree C} \cdot 55 \degree C = 924 \space 000 \space Дж = 0.0924 \cdot 10^7 \space Дж$.
Теперь рассчитаем количество теплоты, которое выделится при сгорании керосина:$Q_к = q_к m_к$,$Q_к = 4.6 \cdot 10^7 \frac{Дж}{кг} \cdot 0.05 \space кг = 0.23 \cdot 10^7 \space Дж$.
Подставим найденные значения в формулу для расчета КПД:$\eta = \frac{0.0924 \cdot 10^7 \space Дж}{0.23 \cdot 10^7 \space Дж} \cdot 100\% \approx 0.402 \cdot 100 \% \approx 40.2 \%$.
Ответ: $\eta \approx 40.2 \%$.
Задача №5
При сжигании смеси, состоящей из бурого угля и каменного угля, выделилось количество теплоты, равное $78.2 \space МДж$. Какая масса бурого угля содержалась в смеси, если известно, что она была в 2 раза больше, чем масса каменного? Удельная теплота сгорания бурого угля составляет $1.5 \cdot 10^7 \frac{Дж}{кг}$.
Дано:$Q = 78.2 \space МДж$$m_1 = 2m_2$$q_1 = 1.5 \cdot 10^7 \frac{Дж}{кг}$$q_2 = 2.7 \cdot 10^7 \frac{Дж}{кг}$
СИ:$Q = 7.82 \cdot 10^7 \space Дж$
$m_1 — ?$
Показать решение и ответ
Скрыть
Решение:
При сгорании бурого угля, содержащегося в смеси, выделилось количество теплоты:$Q_1 = q_1 m_1$.
При сгорании каменного угля, содержащегося в смеси, выделилось количество теплоты:$Q_2 = q_2 m_2$.
Эти величины составляют общее количество теплоты $Q$, которое выделяется при сгорании смеси:$Q = Q_1 +Q_2$.$Q = q_1 m_1 + q_2 m_2$.
Выразим массу каменного угля через массу бурого и подставим в формулу: $m_2 = \frac{m_1}{2}$,$Q = q_1 m_1 + \frac{q_2 m_1}{2}$.
Выразим отсюда искомую массу бурого угля:$Q = m_1 \cdot (q_1 + \frac{q_2}{2})$,$m_1 = \frac{Q}{q_1 + \frac{q_2}{2}}$.
Рассчитаем эту массу:$m_1 = \frac{7.82 \cdot 10^7 \space Дж}{1.5 \cdot 10^7 \frac{Дж}{кг} + \frac{2.7 \cdot 10^7 \frac{Дж}{кг}}{2}} = \frac{7.82 \cdot 10^7 \space Дж}{2.85 \cdot 10^7 \frac{Дж}{кг}} \approx 2.7 \space кг$.
Ответ: $m_1 \approx 2.7 \space кг$.
Задача № 1
Условие. Температура металла изменяется от 20 до 24 градусов Цельсия. При этом его внутренняя энергия увеличилась на 152 Дж. Чему равна удельная теплоемкость металла, если его масса равна 100 граммам?
Решение. Для нахождения ответа потребуется воспользоваться формулой, записанной под номером 1. Все величины, необходимые для расчетов, есть. Только сначала необходимо перевести массу в килограммы, иначе ответ получится неправильный. Потому что все величины должны быть такими, которые приняты в СИ.
В одном килограмме 1000 граммов. Значит, 100 граммов нужно разделить на 1000, получится 0,1 килограмма.
Подстановка всех величин дает такое выражение: с = 152 / (0,1 * (24 – 20)). Вычисления не представляют особой трудности. Результатом всех действий является число 380.
Ответ: с = 380 Дж/(кг * ºС).
Задача №2
Заряд пороха в патроне пулемета имеет массу $3.2 \space г$. Теплота сгорания пороха равна $3.8 \frac{МДж}{кг}$. Сколько выделяется тепла при каждом выстреле?
Дано:$q = 3.8 \frac{МДж}{кг}$$m = 3.2 \space г$
СИ:$q = 3.8 \cdot 10^6 \frac{Дж}{кг}$$m = 3.2 \cdot 10^{-3} \space кг$
$Q — ?$
Показать решение и ответ
Скрыть
Решение:
Формула для расчета количества теплоты, выделяющегося при сгорании топлива:$Q = qm$.
Подставим в формулу известные величины и рассчитаем количество теплоты:$Q = 3.8 \cdot 10^6 \frac{Дж}{кг} \cdot 3.2 \cdot 10^{-3} \space кг = 12.16 \cdot 10^3 \space Дж \approx 12.16 \space кДж$.
Такое количество теплоты выделяется при каждом выстреле.
Ответ: $Q \approx 12.16 \space кДж$.
Задача №6
Какой объем природного газа сгорает в газовой горелке кухонной плиты при нагревании $10 \space л$ воды от температуры $10 \degree C$ до температуры $100 \degree C$, если на нагревание воды идет $r = 60 \%$ выделяющейся при сгорании энергии?
При записи условий задачи, обозначим все величины, связанные с водой, нижним индексом “в”, а с природным газом — “г”.
Дано:$V_в = 10 \space л$$\rho_в = 1000 \frac{кг}{м^3}$$t_1 = 10 \degree C$$t_2 = 100 \degree C$$c_в = 4200 \frac{Дж}{кг \cdot \degree}$$q_г = 4.4 \cdot 10^7 \frac{Дж}{кг}$$\rho_г = 0.8 \frac{кг}{м^3}$$r = 60 \%$
СИ:$V_в = 10^{-2} \space м^3$
$V_г — ?$
Показать решение и ответ
Скрыть
Решение:
Сначала нам нужно рассчитать количество теплоты, которое необходимо сообщить воде, чтобы нагреть ее от $10 \degree C$ до $100 \degree C$:$Q_в = c_в m_в (t_2 — t_1)$.
Выразим массу воды через ее плотность и объем:$m_в = \rho_в V_в$.
Подставим ее в формулу и рассчитаем количество теплоты:$Q_в = c_в \rho_в V_в (t_2 — t_1)$,$Q_в = 4200 \frac{Дж}{кг \cdot \degree} \cdot 1000 \frac{кг}{м^3} \cdot 10^{-2} \space м^3 \cdot (100 \degree C — 10 \degree C) = 42 \space 000 \frac{Дж}{\degree C} \cdot 90 \degree C = 3.78 \cdot 10^6 \space Дж$.
Количество теплоты, выделяемой при сгорании природного газа, вычисляется по формуле:$Q_г = q_г m_г$.
Выразим массу через плотность и объем и подставим в эту формулу:$m_г = \rho_г V_г$,$Q_г = q_г \rho_г V_г$.
В условии задача сказано, что на нагревание идет всего $60 \%$ энергии, выделяемой при сгорании газа:$Q_г \cdot 60 \% = Q_в$.
Подставим сюда выражение для количества теплоты, выделяемого при сгорании природного газа:$q_г \rho_г V_г \cdot 60 \% = Q_в$.
Выразим отсюда объем природного газа:$V_г = \frac{Q_в}{q_г \rho_г \cdot 60 \%}$.
Рассчитаем его:$V_г = \frac{3.78 \cdot 10^6 \space Дж}{4.4 \cdot 10^7 \frac{Дж}{кг} \cdot 0.8 \frac{кг}{м^3} \cdot 60 \%} = \frac{3.78 \cdot 10^6 \space Дж}{2.112 \cdot 10^7 \frac{Дж}{м^3}} = \frac{0.378 \cdot 10^7 \space Дж}{2.112 \cdot 10^7 \frac{Дж}{м^3}} \approx 0.18 \space м^3$.
Ответ: $V_г \approx 0.18 \space м^3$.
Задача № 3
Условие. Имеется химический стакан массой 100 г. В него налито 50 г воды. Начальная температура воды со стаканом равна 0 градусам Цельсия. Какое количество теплоты потребуется для того, чтобы довести воду до кипения?
Решение. Начать стоит с того, чтобы ввести подходящее обозначение. Пусть данные, относящиеся к стакану, будут иметь индекс 1, а к воде — индекс 2. В таблице необходимо найти удельные теплоемкости. Химический стакан сделан из лабораторного стекла, поэтому его значение с1 = 840 Дж/ (кг * ºС). Данные для воды такие: с2 = 4200 Дж/ (кг * ºС).
Их массы даны в граммах. Требуется перевести их в килограммы. Массы этих веществ будут обозначены так: m1 = 0,1 кг, m2 = 0,05 кг.
Начальная температура дана: t1 = 0 ºС. О конечной известно, что она соответствует той, при которой вода кипит. Это t2 = 100 ºС.
Поскольку стакан нагревается вместе с водой, то искомое количество теплоты будет складываться из двух. Первой, которая требуется для нагревания стекла (Q1), и второй, идущей на нагревание воды (Q2). Для их выражения потребуется вторая формула. Ее необходимо записать два раза с разными индексами, а потом составить их сумму.
Получается, что Q = с1 * m1 * (t2 – t1) + с2 * m2 * (t2 – t1). Общий множитель (t2 – t1) можно вынести за скобку, чтобы было удобнее считать. Тогда формула, которая потребуется для расчета количества теплоты, примет такой вид: Q = (с1 * m1 + с2 * m2) * (t2 – t1). Теперь можно подставить известные в задаче величины и сосчитать результат.
Q = (840 * 0,1 + 4200 * 0,05) * (100 – 0) = (84 + 210) * 100 = 294 * 100 = 29400 (Дж).
Ответ. Q = 29400 Дж = 29,4 кДж.
Термохимическое уравнение
Химические уравнения, в которых отображается тепловой эффект называются термохимическими. При записи в скобках обязательно указывают агрегатное состояние вещества: твердое, жидкое, газообразное и другое. Коэффициенты прописываются в условии: дробные или цельные числа.
При расчете учитывают температуру и давление, при которых протекает процесс. Если в условиях задачи не прописаны значения, то их принимают как стандартные: температура 278К, а давление 110,3 кПа.
В конце записи химического уравнения записывают значение Q, которое берут в справочнике, отдельно для каждого вещества. Энергия представлена в кДж в стандартных условиях. Применяется для расчета по формулам.
Расчёт
Выполним расчёт CP воды и олова при следующих условиях:
- m = 500 грамм;
- t1 =24ºC и t2 = 80ºC – для воды;
- t1 =20ºC и t2 =180ºC – для олова;
- Q = 28 тыс. Дж.
Для начала определяем ΔT для воды и олова соответственно:
- ΔТв = t2–t1 = 80–24 = 56ºC
- ΔТо = t2–t1 = 180–20 =160ºC
Затем находим удельную теплоёмкость:
- с=Q/(m*ΔТв)= 28 тыс. Дж/(500 г *56ºC) = 28 тыс.Дж/(28 тыс.г*ºC) = 1 Дж/г*ºC.
- с=Q/(m*ΔТо)=28тыс.Дж/(500 гр*160ºC)=28 тыс.Дж/(80 тыс.г*ºC)=0,35 Дж/г*ºC.
Таким образом, удельная теплоемкость воды составила 1 Дж/г *ºC, а олова 0,35 Дж/г*ºC. Отсюда можно сделать вывод о том, что при равном значении подводимого тепла в 28 тыс. Дж олово нагрется быстрее воды, поскольку его теплоёмкость меньше.
Теплоёмкостью обладают не только газы, жидкости и твёрдые тела, но и продукты питания.
Формула
Перед тем, как приступить к непосредственному расчёту параметра следует ознакомиться с формулой и её компонентами.
Формула для расчёта удельной теплоёмкости имеет следующий вид:
с = Q/(m*∆T)
Знание величин и их символических обозначений, использующихся при расчёте, крайне важно. Однако необходимо не только знать их визуальный вид, но и чётко представлять значение каждого из них
Расчёт удельной теплоёмкости вещества представлен следующими компонентами:
ΔT – символ, означающий постепенное изменение температуры вещества. Символ «Δ» произносится как дельта.
ΔT можно рассчитать по формуле:
ΔT = t2–t1, где
- t1 – первичная температура;
- t2 – конечная температура после изменения.
m – масса вещества используемого при нагреве (гр).
Q – количество теплоты (Дж/J)
На основании Цр можно вывести и другие уравнения:
- Q = m*цp*ΔT – количество теплоты ;
- m = Q/цр*(t2 — t1) – массы вещества;
- t1 = t2–(Q/цp*m) – первичной температуры;
- t2 = t1+(Q/цp*m) – конечной температуры.
Как перевести джоули в метры?
Укажите значения ниже, чтобы преобразовать джоуль в ньютон-метр или наоборот. … Таблица перевода Джоуль в Ньютон-метр.
| Джоуль | Ньютон-метр |
|---|---|
| 0.01 J | 0.01 Н * м |
| 0.1 J | 0.1 Н * м |
| 1 J | 1 Н * м |
| 2 J | 2 Н * м |
Килоджоули меньше джоулей? Таким образом, килоджоуль (кДж) — это 1000 джоулей, а мегаджоуль (МДж) — это 1,000,000 джоулей. Связанная единица — это ватт, который представляет собой единицу мощности (энергии в единицу времени).
Как перевести джоули в кДж моль?
Принятые книжные энтальпии выражены в единицах кДж/моль. Просто конвертируйте J в kJ делением на 1000. Поскольку 1 кДж = 1000 Дж. Вы должны использовать моли продукта.
Как Манг Джи в КГ? Килограмм равен 1000 грамм.
Таблица удельных теплоемкостей
Удельная теплоемкость — табличная величина. Часто ее указывают в условии задачи, но при отсутствии в условии — можно и нужно воспользоваться таблицей. Ниже приведена таблица удельных теплоемкостей для некоторых (многих) веществ.
|
Газы |
C, Дж/(кг·К) |
|
Азот N2 |
1051 |
|
Аммиак NH3 |
2244 |
|
Аргон Ar |
523 |
|
Ацетилен C2H2 |
1683 |
|
Водород H2 |
14270 |
|
Воздух |
1005 |
|
Гелий He |
5296 |
|
Кислород O2 |
913 |
|
Криптон Kr |
251 |
|
Ксенон Xe |
159 |
|
Метан CH4 |
2483 |
|
Неон Ne |
1038 |
|
Оксид азота N2O |
913 |
|
Оксид азота NO |
976 |
|
Оксид серы SO2 |
625 |
|
Оксид углерода CO |
1043 |
|
Пропан C3H8 |
1863 |
|
Сероводород H2S |
1026 |
|
Углекислый газ CO2 |
837 |
|
Хлор Cl |
520 |
|
Этан C2H6 |
1729 |
|
Этилен C2H4 |
1528 |
|
Металлы и сплавы |
C, Дж/(кг·К) |
|
Алюминий Al |
897 |
|
Бронза алюминиевая |
420 |
|
Бронза оловянистая |
380 |
|
Вольфрам W |
134 |
|
Дюралюминий |
880 |
|
Железо Fe |
452 |
|
Золото Au |
129 |
|
Константан |
410 |
|
Латунь |
378 |
|
Манганин |
420 |
|
Медь Cu |
383 |
|
Никель Ni |
443 |
|
Нихром |
460 |
|
Олово Sn |
228 |
|
Платина Pt |
133 |
|
Ртуть Hg |
139 |
|
Свинец Pb |
128 |
|
Серебро Ag |
235 |
|
Сталь стержневая арматурная |
482 |
|
Сталь углеродистая |
468 |
|
Сталь хромистая |
460 |
|
Титан Ti |
520 |
|
Уран U |
116 |
|
Цинк Zn |
385 |
|
Чугун белый |
540 |
|
Чугун серый |
470 |
|
Жидкости |
Cp, Дж/(кг·К) |
|
Азотная кислота (100%-ная) NH3 |
1720 |
|
Бензин |
2090 |
|
Вода |
4182 |
|
Вода морская |
3936 |
|
Водный раствор хлорида натрия (25%-ный) |
3300 |
|
Глицерин |
2430 |
|
Керосин |
2085…2220 |
|
Масло подсолнечное рафинированное |
1775 |
|
Молоко |
3906 |
|
Нефть |
2100 |
|
Парафин жидкий (при 50С) |
3000 |
|
Серная кислота (100%-ная) H2SO4 |
1380 |
|
Скипидар |
1800 |
|
Спирт метиловый (метанол) |
2470 |
|
Спирт этиловый (этанол) |
2470 |
|
Топливо дизельное (солярка) |
2010 |
Задача
Какое твердое вещество массой 2 кг можно нагреть на 10 ˚C, сообщив ему количество теплоты, равное 7560 Дж?
Решение:
Используем формулу для нахождения удельной теплоемкости вещества:
c= Q/m(tконечная — tначальная)
Подставим значения из условия задачи:
c= 7560/2*10 = 7560/20 = 378 Дж/кг*˚C
Смотрим в таблицу удельных теплоемкостей для металлов и находим нужное значение.
|
Металлы и сплавы |
C, Дж/(кг·К) |
|
Алюминий Al |
897 |
|
Бронза алюминиевая |
420 |
|
Бронза оловянистая |
380 |
|
Вольфрам W |
134 |
|
Дюралюминий |
880 |
|
Железо Fe |
452 |
|
Золото Au |
129 |
|
Константан |
410 |
|
Латунь |
378 |
|
Манганин |
420 |
|
Медь Cu |
383 |
|
Никель Ni |
443 |
|
Нихром |
460 |
|
Олово Sn |
228 |
|
Платина Pt |
133 |
|
Ртуть Hg |
139 |
|
Свинец Pb |
128 |
|
Серебро Ag |
235 |
|
Сталь стержневая арматурная |
482 |
|
Сталь углеродистая |
468 |
|
Сталь хромистая |
460 |
|
Титан Ti |
520 |
|
Уран U |
116 |
|
Цинк Zn |
385 |
|
Чугун белый |
540 |
|
Чугун серый |
470 |
Ответ: латунь
составить термохимическое уравнение
Взаимодействие веществ принято отражать (записывать) с помощью химического уравнения. Если в таком уравнении указан тепловой эффект, то тогда уравнение будет называться .
Например, обычное уравнение реакции:
А это уже термохимическое уравнение данной реакции:
Уравнение говорит о том, что при взаимодействии 1 моля PbO с 1 молем СО, идущем с образованием 1 моля Pb и 1 моля CO2, выделяется 64 кДж теплоты.
Особенности термохимических уравнений:
1) указывается агрегатное состояние веществ (однако, если все вещества находятся в одном агрегатном состоянии, то его могут не указывать);
2) указывается тепловой эффект реакции в соответствии с ее стехиометрией (то есть, в соответствии с правильно расставленными коэффициентами);
3) тепловой эффект записывается в левой части уравнения;
4) если речь идет о горении вещества, то уравнение составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции называется
5) если речь идет об образовании вещества, то уравнение также составляется по отношению к 1 молю этого вещества; тепловой эффект такой реакции будет называться
А теперь разберем несколько задач, требованием которых является составление термохимического уравнения.
Что нужно сделать для решения таких задач?
1) записать условие задачи;
2) составить уравнение реакции;
3) вычислить ее тепловой эффект;
4) записать полученное значение теплового эффекта в уравнение реакции.
Пример 1. Кальций массой 8 г сгорает с выделением 127 кДж теплоты. Напишите термохимическое уравнение (тху) реакции.
Пример 2. При разложении 6,86 г оксида ртути (II) тратится 3,64 кДж тепловой энергии. Напишите термохимическое уравнение (тху) реакции.
Пример 3. Реакция 6 г углерода с водородом приводит к выделению 37,42 кДж теплоты. Напишите термохимическое уравнение (тху) реакции образования метана.
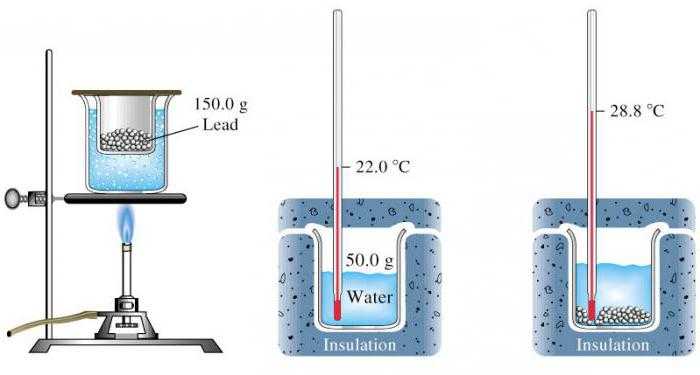
В чем заключается лабораторная работа по измерению удельной теплоемкости?
В школьном курсе физики ее определяют для твердого тела. Причем его теплоемкость высчитывается благодаря сравнению с той, которая известна. Проще всего это реализуется с водой.

В процессе выполнения работы требуется измерить начальные температуры воды и нагретого твердого тела. Потом опустить его в жидкость и дождаться теплового равновесия. Весь эксперимент проводится в калориметре, поэтому потерями энергии можно пренебречь.
Потом требуется записать формулу количества теплоты, которое получает вода при нагревании от твердого тела. Второе выражение описывает энергию, которую отдает тело при остывании. Эти два значения равны. Путем математических вычислений остается определить удельную теплоемкость вещества, из которого состоит твердое тело.
Чаще всего ее предлагается сравнить с табличными значениями, чтобы попытаться угадать, из какого вещества сделано изучаемое тело.
Виды теплопередачи
Теплопередача — процесс передачи теплоты (обмена энергией).
Здесь все совсем несложно, видов всего три: теплопроводность, конвекция и излучение.
Теплопроводность
Тот вид теплопередачи, который можно охарактеризовать, как способность тел проводить энергию от более нагретого тела к менее нагретому.
Речь о том, чтобы передать тепло с помощью соприкосновения. Признавайтесь, грелись же когда-нибудь возле батареи. Если вы сидели к ней вплотную, то согрелись вы благодаря теплопроводности. Обниматься с котиком, у которого горячее пузо, тоже эффективно.
Порой мы немного перебарщиваем с возможностями этого эффекта, когда на пляже ложимся на горячий песок. Эффект есть, только не очень приятный. Ну а ледяная грелка на лбу дает обратный эффект — ваш лоб отдает тепло грелке.
Конвекция
Когда мы говорили о теплопроводности, мы приводили в пример батарею. Теплопроводность — это когда мы получаем тепло, прикоснувшись к батарее. Но все вещи в комнате к батарее не прикасаются, а комната греется. Здесь вступает конвекция.
Дело в том, что холодный воздух тяжелее горячего (холодный просто плотнее). Когда батарея нагревает некий объем воздуха, он тут же поднимается наверх, проходит вдоль потолка, успевает остыть и спуститься обратно вниз — к батарее, где снова нагревается. Таким образом, вся комната равномерно прогревается, потому что все более горячие потоки сменяют все менее холодные.
Излучение
Пляж мы уже упоминали, но речь шла только о горячем песочке. А вот тепло от солнышка — это излучение. В этом случае тепло передается через волны.
Если мы греемся у камина, то получаем тепло конвекцией или излучением?
Обоими способами. То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
Задача №1
Какое количество теплоты выделится при сгорании керосина массой $300 \space г$?
Дано:$m = 300 \space г$$q = 4.6 \cdot 10^7 \frac{Дж}{кг}$
СИ:$m = 0.3 \space кг$
$Q — ?$
Показать решение и ответ
Скрыть
Решение:
Формула для расчета количества теплоты, выделяющегося при сгорании топлива:$Q = qm$.
Подставим в формулу известные величины и рассчитаем количество теплоты:$Q = 4.6 \cdot 10^7 \frac{Дж}{кг} \cdot 0.3 \space кг = 1.38 \cdot 10^7 \space Дж = 13.8 \cdot 10^6 \space Дж = 13.8 \space МДж$.
В таких простых задачах обращайте внимание на размерность исходных величин, не забывайте переводить их в СИ (как мы перевели $г$ в $кг$). При простом решении можно получить неправильный ответ, пропустив размерность используемых величин
Ответ: $Q = 13.8 \space MДж$.
Закон Гесса
В 1840 году русский ученый описал закон термохимии, который до сих пор используется. Его называют законом Гесса:
Тепловой эффект зависит от агрегатного состояния начальных и конечных продуктов, промежуточные стадии, не влияют.
Это правило помогает узнать тепловой эффект промежуточных стадий. Он будет равен разнице между начальным и конечным значением. По сумме переходных реакций выясняют общий тепловой эффект.
Тепловой эффект химических реакций
Количество теплоты, которые выделяется или поглощается в результате реакции, называют тепловым эффектом данной реакции.
- обычно обозначают Q
Qp = Qкон. — Qисх.
- выражают в Дж или кДж
2H2(г) + O2(г) = 2H2O(ж) + 484 кДж
Смотри также:
- Классификация химических реакций в неорганической и органической химии
- Скорость химической реакции, ее зависимость от различных факторов
- Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
- Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты
- Реакции ионного обмена
- Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
- Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее
- Электролиз расплавов и растворов (солей, щелочей, кислот)
- Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии
Что это такое?
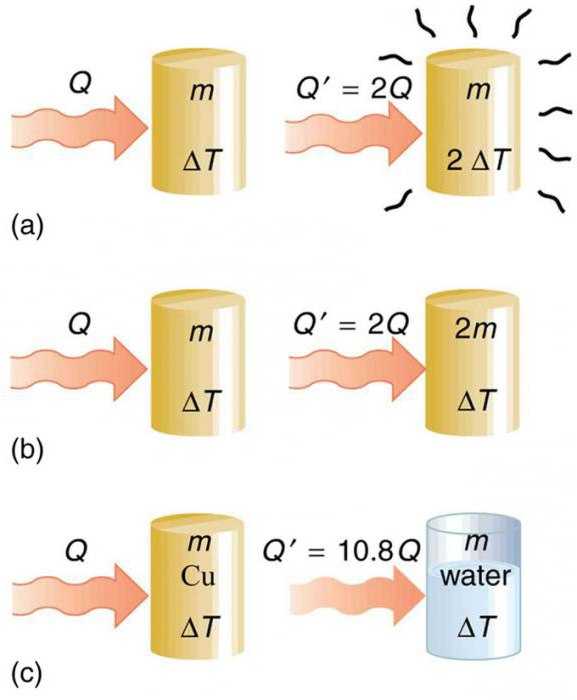
Удельная теплоемкость вещества вводится в тот момент, когда рассматривается ситуация с его нагреванием. Без него невозможно узнать, какое количество теплоты (или энергии) потребуется затратить на этот процесс. А также вычислить ее значение при охлаждении тела. Кстати, эти два количества теплоты равны друг другу по модулю. Но имеют разные знаки. Так, в первом случае она положительная, потому что энергию нужно затратить и она передается телу. Вторая ситуация с охлаждением дает отрицательное число, потому что тепло выделяется, и внутренняя энергия тела уменьшается.
Обозначается эта физическая величина латинской буквой c. Определяется она как некоторое количество теплоты, необходимое для нагревания одного килограмма вещества на один градус. В курсе школьной физики в качестве этого градуса выступает тот, что берется по шкале Цельсия.
Задача № 2
Условие. Определить конечную температуру, до которой остынет вода объемом 5 литров, если она была взята при 100 ºС и выделила в окружающую среду 1680 кДж тепла.
Решение. Начать стоит с того, что энергия дана в несистемной единице. Килоджоули нужно перевести в джоули: 1680 кДж = 1680000 Дж.
Для поиска ответа необходимо воспользоваться формулой под номером 8. Однако в ней фигурирует масса, а в задаче она неизвестна. Зато дан объем жидкости. Значит, можно воспользоваться формулой, известной как m = ρ * V. Плотность воды равна 1000 кг/ м3. Но здесь объем потребуется подставлять в кубических метрах. Чтобы перевести их из литров, необходимо разделить на 1000. Таким образом, объем воды равен 0,005 м3.
Подстановка значений в формулу массы дает такое выражение: 1000 * 0,005 = 5 кг. Удельную теплоемкость потребуется посмотреть в таблице. Теперь можно переходить к формуле 8: t2 = 100 + (1680000 / 4200 * 5).
Первым действием полагается выполнить умножение: 4200 * 5. Результат равен 21000. Второе — деление. 1680000 : 21000 = 80. Последнее — вычитание: 100 — 80 = 20.
Ответ. t2 = 20 ºС.

































